Muitos Sao Os Exemplos De Processos Exotermicos – Muitos São os Exemplos de Processos Exotérmicos, fenômenos que liberam calor para o ambiente, permeiam o nosso cotidiano e a natureza. Desde a simples combustão de uma vela até a complexa respiração celular, esses processos demonstram a capacidade de gerar energia através da liberação de calor.
A compreensão dos processos exotérmicos é crucial para diversas áreas, desde a indústria até a biologia, e nos permite explorar e utilizar a energia liberada em diversas aplicações.
Processos exotérmicos são caracterizados pela liberação de energia para o ambiente, geralmente na forma de calor. A reação química envolvida nesses processos resulta em uma diminuição da energia interna do sistema, o que se manifesta como um aumento da temperatura do ambiente.
Em contraste, processos endotérmicos absorvem calor do ambiente, resultando em um resfriamento do sistema. Essa diferença fundamental define a natureza dos processos exotérmicos e endotérmicos.
Introdução
Processos exotérmicos são reações químicas ou físicas que liberam calor para o ambiente. Essa liberação de calor é uma característica fundamental desses processos, e é frequentemente observada como um aumento na temperatura do sistema ou do ambiente ao redor.
A liberação de calor em processos exotérmicos é resultado da diferença entre a energia dos reagentes e a energia dos produtos. Quando os reagentes se transformam em produtos, a energia total do sistema diminui, e essa diferença de energia é liberada na forma de calor.
Exemplos do Cotidiano
Processos exotérmicos são comuns em nosso dia a dia, e podemos observá-los em diversas situações.
- A queima de combustíveis, como madeira, gás natural e álcool, é um processo exotérmico que libera calor e luz, sendo utilizado para aquecer ambientes e cozinhar alimentos.
- A explosão de dinamite é um exemplo extremo de reação exotérmica, que libera uma grande quantidade de energia em um curto período de tempo.
- A reação de neutralização de um ácido com uma base também é exotérmica, liberando calor e formando sal e água.
- A respiração celular, processo que ocorre em nosso corpo para obter energia a partir dos alimentos, é um processo exotérmico que libera calor e dióxido de carbono.
Comparação com Processos Endotérmicos
Os processos exotérmicos são o oposto dos processos endotérmicos, que absorvem calor do ambiente.
| Característica | Processos Exotérmicos | Processos Endotérmicos |
|---|---|---|
| Fluxo de calor | Libera calor para o ambiente | Absorve calor do ambiente |
| Variação de entalpia (ΔH) | Negativa (ΔH < 0) | Positiva (ΔH > 0) |
| Temperatura | Aumenta a temperatura do sistema ou do ambiente | Diminui a temperatura do sistema ou do ambiente |
| Exemplos | Queima de combustíveis, explosões, neutralização de ácidos e bases | Fusão de gelo, evaporação de água, fotossíntese |
Exemplos de Processos Exotérmicos na Natureza
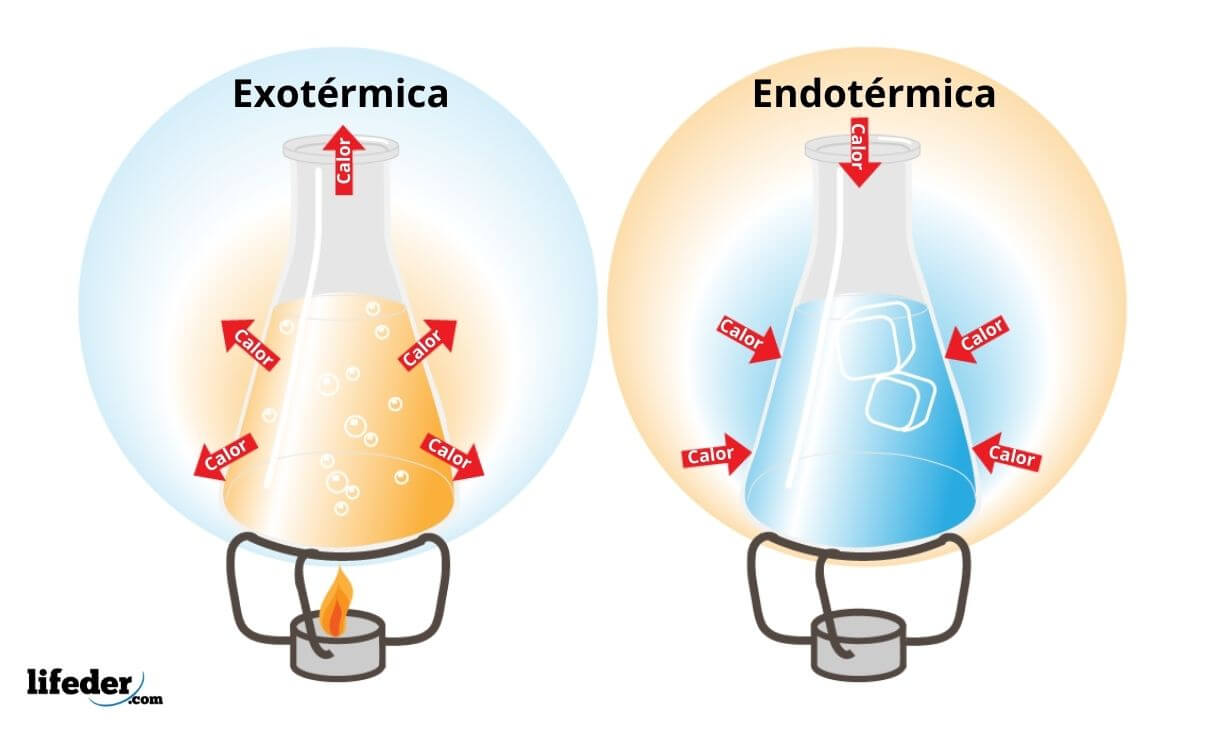
Os processos exotérmicos são comuns na natureza e desempenham um papel fundamental em diversos fenômenos, liberando energia para o ambiente. A combustão, a respiração celular e a reação de neutralização são exemplos notáveis de processos exotérmicos que ocorrem naturalmente, com importantes implicações para a vida e o meio ambiente.
Combustão
A combustão é um processo químico exotérmico que envolve a reação rápida entre uma substância combustível e um oxidante, geralmente oxigênio, liberando calor e luz. Essa reação é caracterizada pela formação de novas substâncias, como dióxido de carbono (CO 2) e água (H 2O), e pela liberação de energia na forma de calor e luz.
A reação de combustão de um hidrocarboneto, como o metano (CH4), pode ser representada pela seguinte equação química:CH 4+ 2O 2→ CO 2+ 2H 2O + Energia
A combustão é um processo fundamental para a geração de energia em diversas áreas, como a produção de eletricidade em usinas termoelétricas e o funcionamento de motores a combustão interna. A queima de combustíveis como madeira, gás natural e petróleo libera energia térmica, que pode ser utilizada para diversos fins.
Respiração Celular, Muitos Sao Os Exemplos De Processos Exotermicos
A respiração celular é um processo biológico exotérmico que ocorre nas células dos organismos vivos, liberando energia química armazenada nos nutrientes, como glicose, para realizar as funções vitais. Esse processo envolve uma série de reações químicas complexas, que podem ser resumidas na seguinte equação geral:
C6H 12O 6+ 6O 2→ 6CO 2+ 6H 2O + Energia (ATP)
A energia liberada na respiração celular é armazenada na forma de adenosina trifosfato (ATP), a principal moeda energética das células. Essa energia é utilizada para diversas funções celulares, como o crescimento, o movimento, a síntese de proteínas e o transporte de substâncias.
Reação de Neutralização
A reação de neutralização entre ácidos e bases é um processo exotérmico que envolve a liberação de calor. Quando um ácido reage com uma base, os íons hidrogênio (H +) do ácido reagem com os íons hidróxido (OH –) da base, formando água (H 2O) e liberando calor.
Por exemplo, a reação de neutralização entre o ácido clorídrico (HCl) e o hidróxido de sódio (NaOH) pode ser representada pela seguinte equação química:HCl + NaOH → NaCl + H2O + Calor
A reação de neutralização é utilizada em diversas aplicações, como a produção de sais, a regulação do pH de soluções e a neutralização de ácidos e bases em efluentes industriais.
Aplicações de Processos Exotérmicos: Muitos Sao Os Exemplos De Processos Exotermicos

Os processos exotérmicos, que liberam calor para o ambiente, desempenham um papel fundamental em diversas áreas da vida moderna, desde a produção de energia até a fabricação de produtos essenciais.
Utilização em Indústrias
As reações exotérmicas são amplamente utilizadas na indústria para gerar energia e calor. Um exemplo notável é a produção de energia em usinas termoelétricas. Nesses locais, combustíveis como carvão, gás natural ou petróleo são queimados em reações exotérmicas, liberando calor que é utilizado para gerar vapor.
Esse vapor, por sua vez, movimenta turbinas que geram eletricidade. As usinas termoelétricas são responsáveis por uma parcela significativa da produção de energia global.
Reações Químicas Exotérmicas
Os processos exotérmicos são utilizados em diversas reações químicas para gerar calor e energia. Por exemplo, a combustão de combustíveis, como a madeira e o gás natural, é uma reação exotérmica que libera calor e luz. Essa energia pode ser utilizada para cozinhar, aquecer casas e operar motores.
Outro exemplo é a reação de neutralização entre ácidos e bases, que libera calor e forma sal e água.
Aplicações em Tecnologias
As reações exotérmicas também desempenham um papel crucial em diversas tecnologias. A soldagem, por exemplo, é um processo que utiliza o calor gerado por reações exotérmicas para fundir metais e unir peças. A soldagem a gás, por exemplo, utiliza a chama de um maçarico para fundir os metais, enquanto a soldagem por arco elétrico utiliza o calor gerado por um arco elétrico.
Outro exemplo importante é a fabricação de explosivos. Explosivos são compostos que, quando detonados, sofrem reações exotérmicas extremamente rápidas, liberando uma grande quantidade de energia em um curto período de tempo. Essa energia é utilizada para realizar tarefas como demolições, mineração e atividades militares.
A Importância dos Processos Exotérmicos

Os processos exotérmicos desempenham um papel fundamental na vida na Terra, fornecendo energia essencial para sustentar organismos vivos e impulsionar inúmeros processos naturais e tecnológicos.
A liberação de energia em reações exotérmicas é crucial para a sobrevivência dos seres vivos. Por exemplo, a respiração celular, um processo exotérmico que ocorre em todas as células vivas, libera energia química armazenada nos alimentos, permitindo que os organismos realizem funções vitais como crescimento, movimento e reprodução.
Além disso, a combustão de combustíveis como madeira e gás natural, que são reações exotérmicas, fornece energia para gerar eletricidade, aquecer residências e alimentar veículos, impactando diretamente a sociedade moderna.
Aplicações dos Processos Exotérmicos
Os processos exotérmicos têm aplicações vastas e diversificadas em diversas áreas, desde a produção de energia até a síntese de novos materiais. A tabela a seguir ilustra algumas das principais aplicações e seus respectivos processos exotérmicos:
| Processo Exotérmico | Aplicações |
|---|---|
| Combustão | Geração de energia elétrica, aquecimento de residências, propulsão de veículos |
| Reações de neutralização | Produção de calor em reações químicas, síntese de compostos |
| Explosões | Mineração, demolição, produção de energia em propulsores de foguetes |
| Reações de polimerização | Produção de plásticos, fibras sintéticas, adesivos |
“Os processos exotérmicos são a força motriz por trás de inúmeros avanços tecnológicos e garantem a energia necessária para sustentar a vida na Terra.”
FAQ Corner
Quais são as principais características de um processo exotérmico?
As principais características de um processo exotérmico são a liberação de calor para o ambiente, a diminuição da energia interna do sistema e a formação de produtos com menor energia interna em relação aos reagentes.
Como posso identificar um processo exotérmico na prática?
Um processo exotérmico é geralmente identificado pela liberação de calor, que pode ser percebida como um aumento da temperatura do sistema ou do ambiente. Além disso, a ocorrência de luz, chama ou explosão pode indicar a liberação de energia em um processo exotérmico.

